La industria farmacéutica convierte a España en una potencia en ensayos clínicos
La anticipación a la normativa europea es bien recibida por los laboratorios En el último año crece un 18% la I+D de las compañías con hospitales
España se ha convertido en un punto caliente en el mundo para los ensayos clínicos de medicamentos innovadores. Las grandes multinacionales de la industria farmacéutica han acelerado en los últimos meses su apuesta por invertir en estas investigaciones en hospitales en el país, aprovechando la calidad del sistema sanitario público y los cambios legislativos que han allanado el camino.
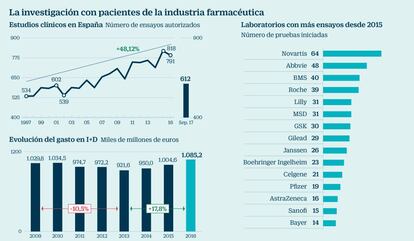
El pasado año la industria farmacéutica llegó a un récord de inversión en I+D en España, que alcanzó los 1.085 millones de euros, un 8% más que en 2015, según los datos facilitados por la patronal Farmaindustria. Más de la mitad (577 millones) se dedicó a ensayos clínicos. Este incremento estuvo propulsado por el capítulo destinado a la colaboración con centros de investigación y hospitales, que creció un 18%. Este sector es muy dependiente de la innovación y suma el 20% del total destinado a I+D en España por todos los sectores industriales.
Las compañías farmacéuticas cuentan con un modelo de negocio en el que es crucial el lanzamiento de nuevas terapias, que son las que además de aportar beneficios para los pacientes cuentan con precios más elevados y un derecho de exclusividad del uso de la patente durante 10 años. Para el desarrollo de esos tratamientos son necesarios los ensayos clínicos, es decir, las pruebas en pacientes de esos medicamentos, realizados en hospitales por médicos.
Diferentes estudios señalan que cada compañía farmacéutica debe gastar cientos de millones en la investigación de un tratamiento. El cálculo más abultado es el de la Universidad de Tufts –que suele considerarse como el referente en el sector–, que en 2014 estimó en 2.500 millones de dólares (2.120 millones de euros) la cuantía de la inversión por cada medicamento que llega al mercado. Este alto coste se debe al gran porcentaje de terapias que fallan por el camino y también por la enorme cantidad de recursos que las empresas deben destinar a probar los fármacos con miles de pacientes simultáneamente en decenas de hospitales en varios países.
Esta industria cada vez es más dependiente de los avances terapéuticos, por lo que la cifra destinada a la I+D no deja de crecer. En Europa invirtió 33.550 millones en 2015 (un incremento del 192% en dos décadas), en EE UU otros 47.000 millones (296% más) y en Japón 14.500 millones (127%).
“España es un país excelente para los ensayos clínicos porque se ha trabajado mucho en los últimos años. De hecho, durante la crisis no ha dejado de crecer el número de estos estudios”, opina Amelia Martín Uranga, responsable de la Plataforma de Medicamentos Innovadores de Farmaindustria. “Europa ha desarrollado una nueva regulación sobre ensayos clínicos que se aprobará el año que viene, pero España ha decidido adelantarse, lo que ha provocado que se simplifiquen los procesos y haya una reducción en los tiempos”, añade.
En los últimos años, la industria ha acelerado el ritmo de ensayos desde los 534 autorizados por la Agencia Española de Medicamentos (Aemps) en 1997 hasta los 791 del pasado año (con un máximo de 818 del 2015).
“Hay un primer salto numérico a principios de esta década y un enorme impulso cualitativo con la publicación del actual real decreto de ensayos clínicos en diciembre de 2015, lo que nos convirtió en el primer país europeo en adaptarse al nuevo Reglamento de la UE”, explican desde la Aemps. “Durante mucho tiempo nuestro talón de Aquiles eran los tiempos, la duplicidad de evaluaciones y la firma de los contratos. Llevamos un año trabajando en ello y los tiempos se han reducido en más de un 30%”, añaden.
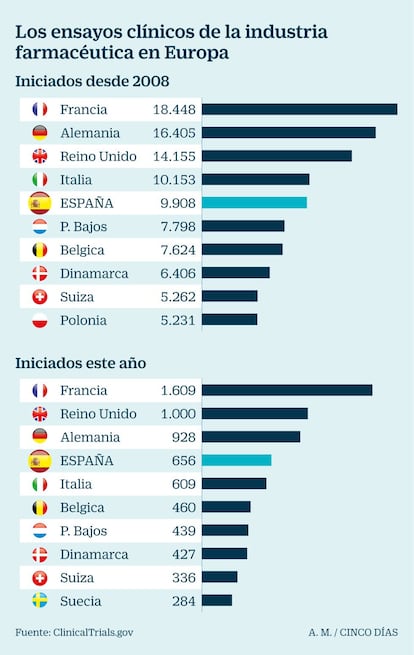
España ocupa el quinto puesto desde 2008 por países con mayor número de ensayos en Europa, según la base de datos pública de Estados Unidos llamada Clinical Trials, que se considera la más completa. Nos superan en estas pruebas con pacientes nuestros vecinos con más población y con potentes farmacéuticas, como Francia –con Sanofi como gran referente europeo–. También Alemania (con grandes empresas como Bayer, Merck o Boehringer Ingelheim), Reino Unido (GSK y AstraZeneca) e Italia. Tras España destacan países más pequeños pero muy potentes en el sector, como Suiza (con los dos gigantes mundiales Roche y Novartis) y Dinamarca (Novo Nordisk y Lundbeck).
En el último año, con datos de Clinical Trials hasta inicios de este mes, España ya ha superado a Italia y ya es el cuarto país, con 656 ensayos. Las previsiones es que ese salto se consolide porque los laboratorios internacionales ven a España como un entorno cada vez más amigable para los ensayos.
Son las multinacionales extranjeras las que están acelerando el paso, ya que de hecho, ningún laboratorio nacional se encuentra entre los 15 con mayor número de estas pruebas con pacientes iniciadas en 2017 y que habitualmente duran varios años. La lista la encabeza Novartis, seguida de Abbvie, BMS, Roche, Lilly, MSD, GSK, Gilead y Janssen, según se recoge en el registro de la Aemps. “España se ha convertido en un caso de éxito”, asegura Martín Uranga.
“España es para nosotros el país número uno en Europa para los ensayos clínicos y el segundo en el mundo detrás de EEUU”, explica Lourdes López-Bravo, directora de ensayos clínicos de la estadounidense MSD. “Se ha convertido en un país muy interesante por la cobertura universal del Sistema Nacional de Salud, la calidad de los profesionales y la presencia de líderes científicos a nivel mundial”, apunta.
López Bravo recuerda además la importancia de esta inyección de recursos para el sistema, ya que los laboratorios sufragan los fármacos administrados en la investigación y forman a los médicos en las innovaciones terapéuticas.
“El beneficio más importante es para los pacientes, a los que se les permite acceder a tratamientos innovadores, y también en la formación de los médicos”, opina Estrella Soriano, directora de investigación clínica de la estadounidense Pfizer.
“España es un buen país para desarrollar investigación clínica, fundamentalmente por la calidad de la ciencia en nuestro país, el trabajo de los investigadores y el marco regulatorio, garantista para los pacientes, pero lo suficientemente ágil”, coincide a Teresa Millán, directora de asuntos corporativos de Lilly. “Creemos que ya somos una referencia mundial, aunque como posible mejora, la disminución de trabas burocráticas para la agilización en los procesos nos ayudaría aún a ser más eficientes”, lamenta.
Coincide en ese punto de vista la responsable de Pfizer: “Hay un cuello de botella en los contratos con los hospitales, ya que varían según cada comunidad autónoma y cada centro”. Esta experta señala también que es necesario mejorar en la profesionalización en los procesos de investigación clínica en algunos hospitales. “Es importante también que los responsables sanitarios tengan claro que no es un gasto, sino una fuente de ingresos porque las empresas pagan por paciente y el fármaco es gratuito”, explica esta experta, quien revela que para Pfizer, España es el segundo país con más ensayos activos (70) en Europa, detrás de Alemania.
“España es un país de referencia en la actividad investigadora de Roche”, asevera también Annarita Gabriele, directora médica de Roche Farma. El laboratorio suizo invierte en I+D en España alrededor de 45 millones de euros. Entre las ventajas que esta responsable percibe, está “el nivel científico de la sanidad española en general”, “los tiempos de inicio de los ensayos clínicos son muy buenos tras el nuevo real decreto que además ha servido para refinar y simplificar el proceso de evaluación”, y las “importantes deducciones fiscales para las empresas por I+D”.
“Creo que una de las mejoras que queda pendiente es la de tener un contrato único con los hospitales. Al tener la sanidad transferidas a las comunidades autónomas, nos encontramos con casos muy diversos”, lamenta la ejecutiva de MSD. “También es importante la estabilidad en España y que las compañías no perciban incertidumbres en el sistema sanitario”, añade.
Desde la Aemps se explica, sobre las divergencias por hospitales, que ya actualmente “se trabaja en generar criterios comunes y de hecho se han publicado documentos para unificar procedimientos en hospitales y comunidades autónomas”.
En España participan más de 800 entidades en estos estudios con pacientes, de los que 469 son hospitales y 325 son centros de salud. En los últimos años, Cataluña lidera el número de pruebas, con el 27% del total, seguida de Madrid (23,3%), Andalucía (12,4%) y Comunidad Valenciana (11,9%). Por patologías, la oncología es claramente el área terapéutica que más ensayos involucra, con el 36,8%. Le siguen otras como cardiovascular, enfermedades infecciosas, neurología, hematología y reumatología.