Pfizer espera distribuir la vacuna del Covid-19 en Europa antes de final de año
Negocia con la Comisión Europea la licitación del contrato de compra Avanza que ya testa un fármaco antiviral como curación y que puede estar listo para el segundo semestre del año que viene
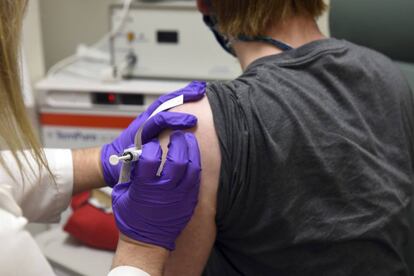

Pfizer tiene muy avanzados los ensayos clínicos de su vacuna frente al coronavirus SARS-CoV-2 y prevé que esa aceleración le permita distribuir la vacuna en la Unión Europea, y por tanto en España, antes de que finalice al año. Así lo avanzó el laboratorio estadounidense este martes en su presentación de resultados del tercer trimestre. Además, la compañía avanza que ya testa un fármaco antiviral como curación del Covid-19 con la intención de tenerlo listo para el segundo semestre del año que viene.
La compañía farmacéutica recuerda que, junto a su socio alemán BioNTech en la I+D de esta inmunización contra el Covid-19, anunció en septiembre que había concluido conversaciones exploratorias con la Comisión Europea (CE) para un suministro de 200 millones de dosis, con una opción para 100 millones de dosis adicionales. "Las entregas comenzarían a fines de 2020, sujetas al éxito clínico y la autorización regulatoria", señalan Pfizer en la presentación a inversores. Este consorcio de empresas se encuentran actualmente en negociaciones de licitación del contrato con el Ejecutivo de Ursula von der Leyen.
En Europa, la Agencia Europea del Medicamento (EMA, en sus siglas en inglés) ya está analizando los estudios de AstraZeneca y Pfizer, pero sin conocerse cuándo se tendrán datos suficientes para una autorización.
La vacuna de Pfizer es una de las 10 candidatas que se prueba en fase III, la última etapa de los ensayos clínicos para testar la eficacia en miles de pacientes. Junto a Pfizer, otras empresas como Janssen, AstraZeneca, Moderna o Curevac cuentan con experimentos avanzados. La empresa de Nueva York prevé fabricar 1.300 millones de dosis para finales de 2021.
España se ha sumado de momento a la compra anticipada que hizo la CE a AstraZeneca, de 300 millones de viales, por lo que proporcionalmente le corresponderán 31,5 millones de dosis. El Ministerio de Sanidad avanzó la semana pasada que espera recibir del laboratorio británico 3,1 millones de vacunas en diciembre. A diferencia de AstraZeneca, Pfizer todavía no ha cerrado el acuerdo con la UE, según apuntaron funcionarios comunitarios recogidos por Reuters por divergencias en como repartir las posibles compensaciones a los ciudadanos en caso de posibles efectos adversos de la vacuna.
EE UU y fabricación
Suponiendo que los datos de los ensayos con voluntarios sean positivos, Pizer anuncia que solicitará aprobación de su producto por la vía de uso de emergencia en EE UU, después de que se logre el hito de seguridad (dos meses de datos de seguridad en la mitad de los participantes después de la dosis final, que ya se ha inyectado a los participantes). En el caso norteamericano, el laboratorio espera esa solicitud de autorización en la tercera semana de noviembre.
Igualmente, el gigante farmacéutica estadounidense espera tener los datos de fabricación listos para su presentación a las autoridades antes de que se alcance el hito de seguridad.
Avances en los ensayos de la vacuna
En septiembre de 2020, Pfizer y BioNTech ampliaron su ensayo hasta aproximadamente 44.000 participantes desde el objetivo inicial de 30.000 participantes. Esa expansión está permitiendo a las empresas aumentar aún más la diversidad de la población con la que se prueba la vacuna experimental y, así, incluir a adolescentes de hasta 16 años y personas con infección crónica y estable por el virus de la inmunodeficiencia humana (VIH), la hepatitis C o la hepatitis B.
Un antiviral experimental
El laboratorio también anuncia que ha comenzado un ensayo clínico de un nuevo antiviral, actualmente en fase I en pruebas con enfermos de Covid-19, para comprobar la seguridad del fármaco. Ese test comenzó en septiembre y la compañía prevé que pueda pasar a fase II/III, para comprobar eficacia, a final de año. "Esperamos presentar para su aprobación en el segundo semestre de 2021", indica la empresa en la presentación a inversores.
Actualmente solo hay aprobado en EE UU y la UE un antiviral como tratamiento frente a esta enfermedad respiratoria, llamado Veklury (remdesivir) del laboratorio Gilead, aunque la Organización Mundial de la Salud a mediados de octubre descartó su eficacia, algo que la compañía farmacéutica rebate.
Impacto de la pandemia en los resultados
La farmacéutica más grande de Estados Unidos, Pfizer, ganó 9.022 millones de dólares hasta septiembre de este año, un 46% menos respecto al mismo periodo de 2019, unos resultados que según la propia compañía "continúan reflejando los impactos comerciales reales y anticipados de la pandemia", sobre todo en sus negocios en China y EE UU.
La facturación en los primeros nueve meses del año también disminuyó un 8%, hasta 35.961 millones de dólares, fundamentalmente por la caída de su división UpJohn, de fármacos maduros, que se deja un 29%.