Fabricantes de originales y genéricos chocan por la dispensa a las patentes
Los laboratorios innovadores temen una caída de la inversión en I+D Aeseg defiende que evitará la deslocalización y creará empleo
Los cambios impulsados por Bruselas en las normas de propiedad intelectual que protegen a los medicamentos han abierto una controversia entre los fabricantes de genéricos y los laboratorios innovadores.
La Comisión Europea propuso en mayo conceder una dispensa a las empresas farmacéuticas para que puedan producir como genéricos moléculas protegidas por patentes, siempre y cuando su destino sea la exportación a mercados fuera de la UE donde la protección haya expirado o nunca haya existido.
La propuesta, que se encuentra en discusión en el Parlamento Europeo, implica modificar el certificado complementario de protección (CCP), un título de propiedad industrial que extiende por un periodo máximo de cinco años la validez de una patente.
El propósito de este instrumento, que la UE adoptó en 1992, es compensar el tiempo perdido por el laboratorio en pruebas clínicas y otros trámites para obtener el permiso de comercialización. La dispensa tendría efecto durante el periodo de vigencia del CCP.
“Actualmente existe un equilibrio entre los intereses de los fabricantes de productos originales y los de genéricos. La exención propuesta por Bruselas rompe ese equilibrio, al mermar los derechos de los laboratorios innovadores”, comentan fuentes de Farmaindustria.
La patronal sostiene que el cambio regulatorio desalentará la inversión en I+D, poniendo a la UE en desventaja frente a competidores como EE UU, Japón y China, país este último que sopesa introducir una norma equivalente al CCP con el fin de atraer inversiones en I+D farmacéutica.
La consultora Clarivate alerta de que competidores como China responderán al cambio en la UE con subida de aranceles
El “debilitamiento” de las leyes europeas de propiedad industrial provocará –advierte la patronal– pérdida de cuota de mercado internacional y de empleo cualificado. “No hay que olvidar que la industria farmacéutica innovadora emplea a 750.000 profesionales en Europa, 115.000 de ellos en tareas de I+D, actividad a la que destina más de 35.000 millones de euros al año”, precisa.
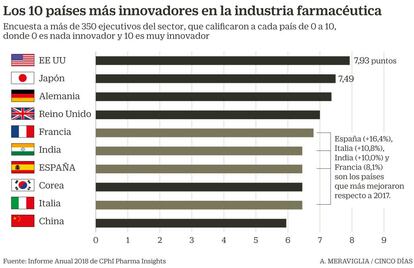
En España, las 154 compañías que integran Farmaindustria (49 de ellas de capital nacional) generan 40.565 puestos directos y gastan cerca de 1.100 millones anuales en investigación. Todo lo cual ha llevado a España a situarse como el séptimo país que más innova en moléculas pequeñas, según el último informe de CPhI presentado en Madrid durante su evento anual.
En cambio, la Asociación Española de Medicamentos Genéricos (Aeseg) defiende que la reforma es necesaria porque la mayoría de patentes vencen en España dos años más tarde que en EE UU y otros países fuera de la UE, lo que obliga a sus empresas a trasladar sus fábricas allí si no quieren perder ese tiempo y cuota de mercado que luego es muy difícil recuperar.
“La medida evitaría la deslocalización de la industria y crearía empleo”, afirma Ángel Luis Rodríguez de la Cuerda, secretario general de Aeseg. Es más, pide que la exención se otorgue también para hacer acopio de existencias suficientes con las cuales abastecer al mercado comunitario desde el día siguiente de expirar la CCP, en lugar de tener que esperar seis meses, que es lo que se tarda en producir un genérico.
Según Medicines for Europe, la representante europea de la industria de los genéricos, la propuesta de Bruselas agregaría 25.000 empleos, 9.500 millones de euros en exportaciones y ahorraría al sistema sanitario de la UE 3.000 millones. “Por el tamaño de su sector, España aportaría entre el 15% y el 20% de esas cifras. Junto con Italia, sería el país más beneficiado”, estima Rodríguez de la Cuerda.
Aeseg defiende los intereses de 13 grupos con fábricas aquí que dan empleo a 9.000 personas y que invierten el 3,5% de sus ingresos en innovación, ya que las patentes normalmente duran 10 años y en ese tiempo se producen avances que deben incorporar a los genéricos.
Almudena Díaz, técnica de patentes de Pons IP, opina que la reforma no debería afectar a la I+D europea, puesto que el periodo de protección de la patente se mantiene intacto para los laboratorios innovadores. Por el contrario, señala que mantener la restricción actual supone una desventaja competitiva para los productores de genéricos y biosimilares de la UE, lo que sí acarrea pérdida de inversiones.
Christopher McKenna, experto de Clarivate Analytics, firma con sede en Filadelfia (EE UU), ve poco probable que la dispensa favorezca demasiado a los productores europeos de genéricos, a menos que pueda usarse para prepararse para el día después de expirar la patente. La razón de su escepticismo es que probablemente los países competidores, como China, responderán a la exención con aumento de aranceles o requisitos de fabricación local.
Desde Farmaindustria coinciden: en Turquía, por ejemplo, se favorece la producción local y no se admiten ciertos medicamentos importados, mientras que Rusia solo acepta productos en cuya fabricación hayan intervenido al menos dos empresas de capital nacional. “El acceso a mercados fuera de la UE es multifactorial y ninguna de las barreras descritas se podrá superar con la exención del CCP”, subrayan.