La EMA relaciona los casos de trombos con la vacuna de Janssen pero recomienda su uso
La Agencia Europea del Medicamento insiste en que los beneficios son superiores a los riesgos
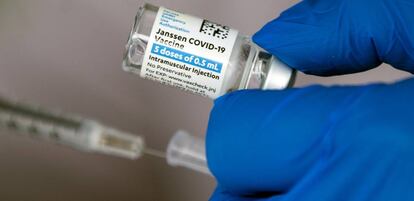

La Agencia Europea del Medicamento ha encontrado relación en los poco frecuentes casos de trombos con la administración de la vacuna de Janssen (grupo Johnson & Jonhson) frente al Covid-19. Así lo asegura el organismo de La Haya en un comunicado emitido este martes, pero como ocurrió en el caso de AstraZeneca insiste en que los beneficios del uso del producto son mayores que los riesgos por este tipo de efectos adversos raros.
Por tanto, abre la vía a que los países administren desde ya este producto monodosis, que no ha llegado a inyectarse a la espera de la respuesta de la EMA. No limita su uso a ningún grupo de edad más allá de los 18 años, por lo que los Gobiernos deberán decidir si, como en el caso de AstraZeneca, lo limitan solo a los mayores de 60 años. En España, se esperan 5,5 millones de estas inyecciones monodosis para este segundo trimestre del año.
La ministra de Sanidad, Carolina Darias, anunció que se procederá "con carácter inmediato" a la distribución a las comunidades autónomas. La compañía, por su parte, indicó que reinicia la distribución de los lotes.
El organismo explica que ha estudiado ocho casos reportados por las autoridades de EE UU sobre más de siete millones de vacunas inyectadas y concluye que la combinación de coágulos sanguíneos y plaquetas bajas en sangre es muy rara, y los beneficios del producto en la prevención del Covid-19 "superan los riesgos de efectos secundarios". La agencia indica que los episodios poco frecuentes de coágulos y bajos niveles de plaquetas deben indicarse en el prospecto del producto.
La vacuna de Johnson & Johnson debería haberse distribuido por primera vez desde la semana pasada, pero se frenó debido a que el grupo americano decidió suspender el reparto hasta que se aclarasen las dudas respecto a posibles casos de trombos como efecto adverso, de forma similar a las consecuencias no deseadas e infrecuentes del producto de AstraZeneca. El 13 de abril, la agencia americana del medicamento (FDA) y los Centros de Control y Prevención de Enfermedades (CDCP, en sus siglas en inglés) de EE UU suspendieron el uso para investigar los casos en el país.
La EMA tomó el mismo camino y avanzó que estudiaría los casos reportados por EE UU, ya que en Europa todavía no se ha comenzado a utilizar, aunque esta vacuna está autorizada desde marzo por Bruselas tras el visto bueno de la agencia del medicamento respecto a seguridad y eficacia.
El comité que ha analizado los informes detalla que todos los casos de trombos se dieron en personas menores de 60 años dentro de las tres semanas posteriores a la vacunación, la mayoría en mujeres. "Según la evidencia actualmente disponible, no se han confirmado factores de riesgo específicos", concluye el organismo.
Estos expertos concluyeron que los coágulos se produjeron en zonas anatómicas inusuales, como en las venas del cerebro (trombosis del seno venoso cerebral) y el abdomen (trombosis de la vena esplácnica) y en las arterias, junto con niveles bajos de plaquetas en sangre y, a veces, se produjo sangrado. "Los casos revisados fueron muy similares a los que ocurrieron con la vacuna del Covid-19 desarrollada por AstraZeneca, Vaxzevria", detalla el comunicado del organismo.
La agencia ofrece una explicación plausible para la combinación de coágulos sanguíneos y plaquetas bajas: "una respuesta inmune, que conduce a una condición similar a la que se observa a veces en pacientes tratados con heparina llamada trombocitopenia inducida por heparina". En cualquier caso, recuerda que la evaluación científica respalda el uso seguro y eficaz de las vacunas aprobadas en Europa. "El uso de la vacuna durante las campañas de vacunación a nivel nacional tendrá en cuenta la situación de la pandemia y la disponibilidad de la vacuna en los distintos Estados miembros", concluye.
Fabricación y distribución
Igual que la de AstraZeneca, esta vacuna está basada en adenovirus y puede conservarse hasta tres meses entre temperaturas de dos a ocho grados centígrados. Janssen busca producir 1.000 millones de su opción monodosis en 2021. En Europa, fabrica el antígeno en Leiden (Países Bajos) y termina el producto en una planta francesa de Sanofi, en otra italiana del proveedor Catalent y, a partir de junio, lo hará en el centro de la farmacéutica cotizada española Reig Jofre en Sant Joan Despí (Barcelona).
La Comisión Europea ha acordado con el gigante estadounidense la compra de 200 millones de dosis, más otros 200 millones adicionales. Para España, corresponden 21 millones de dosis (y la misma cifra opcional).
Más de 80 millones en ingresos
Johnson & Johnson aumentó su beneficio neto un 6,9% en el primer trimestre de 2021 hasta los 6.197 millones de dólares, según anunció este martes el grupo. Los primeros ingresos por su vacuna frente al Covid, aprobada en febrero en EE UU y en marzo en la UE, alcanzaron los 100 millones de dólares (más de 83 millones de euros). En el total de su negocio, el grupo ingresó 22.321 millones de enero a marzo, un 7,9% más que hace un año.